Les
maladies virales sont connues depuis l’Antiquité ( Ernan Cortes et la main de
Dieu, variole ) mais leurs agents, les virus, sont restés inconnus durant très
longtemps. La raison : une taille extrêmement petite, une structure
rudimentaire et des cycles de multiplication très sophistiqués.
Eucaryotes :
un noyau bien délimité, structure très complexe
Procaryotes :
Structure plus simple, un appareil nucléaire diffus, non délimité par une
membrane
Virus :
structure totalement singulière : aucun organites, non vivant, parasites
absolus.
21 – Les éléments de leur structure :
De très petite taille, les virus sont toujours constitués d’un seul type d’acide nucléique et de protéines assemblées de façon complexe et parfois une enveloppe phospholipidique (pas de membrane) :
211 – Leur taille :
Elle
varie de 10 nm à 400 nm pour les plus gros (Poxvirus : variole)
(10
nm = ribosome)
(400
nm = très petite bactérie)
212 – L’acide nucléique ou génome viral :
C’est
un filament d’acide nucléique (ADN ou ARN), stabilisé par des protéines
de structure type histone. Il existe une très grande diversité de génomes
viraux : ADN et ARN simple brin, double brin, linéaire,
circulaire, segmenté etc.
Remarque :
L’ARN
peut avoir une orientation positive ARN (+) : brin codant identique à un
ARN messager donc traduit directement en protéines.
ARN
(+)à
Protéine
L’ARN
peut avoir une orientation négative : l’ARN est alors complémentaire de
l’ARN messager. L’ARN (-) doit d’abord être répliqué en ARN (+)
lors de l’expression génétique.
ARN (-)à
ARN (+)à
Protéine
213 – Les protéines capsidiales :
L’acide
nucléique viral est protégé par une coque rigide formée de protéines :
la capside
La
capside est constituée d’unités protéiques identiques entre elles : les capsomères.
Les
capsomères sont eux mêmes formés d’une ou de plusieurs sous unités protéiques
liées de façon non covalente : les protomères.
Les
capsomères ne s’associent que selon deux types de symétrie :
- symétrie hélicoïdale
- symétrie cubique
|
L’association :
acide nucléique + capside = nucléocapside |
214 – L’enveloppe ou « peplos » :
Bicouche
phospholipidique, vestige de la cellule infectée, dans laquelle on retrouve des
protéines et des glycoprotéines codées par le génome viral.
Elle
joue aussi un rôle dans la reconnaissance par les cellules
lors de la fixation et la libération des virions.
Cette
enveloppe, inconstante chez les virus, possède des propriétés antigéniques
importantes.
215 – Les autres protéines :
Il
est possible de trouver dans la particule virale d’autres protéines de structure
ou des enzymes.
Ces
enzymes joueront un rôle fondamental lors des premières étapes du cycle
infectieux.
Ex :
Transcriptase permet le
passage suivant ARN (-) à
ARN (+)
Reverse Transcriptase (RT) permet le passage suivant : ARN
à ADN !!
22 – Aperçu de la diversité des structures virales :
Suivant
la structure de la capside, on distingue 3 types de symétrie :
221 – Les virus a symétrie cubique :
La
structure de ces virus dérive de l’icosaèdre : 20 faces
(chaque face est représenté par un triangle équilatéral), 12 sommets, 30 arêtes
La
capside est constituée de capsomères eux-mêmes constitués de sous
unités protomères :
- si le capsomère
comporte six protomères : hexons , ils sont disposés sur les faces
- si le capsomères
comporte 5 protomères : pentons , ils sont sur les sommets
Chez
certains virus, les pentons portent des spicules impliqués dans l’attachement
virus - cellules cibles.

Analyse
du document 1A :
1 : protomère
2 : capsomère hexon
3 : capsomère penton
4 : capside
5 : spicule
Analyse
du document 1B :
Analyse
du document 1C :
Exemple : Le VMT (Virus de la Mosaïque du Tabac)
ARN monocaténaire (+), enroulé en hélice
capsoméres tous identiques (2130)
nucléocapside cylindrique avec un espace libre au centre
Analyse
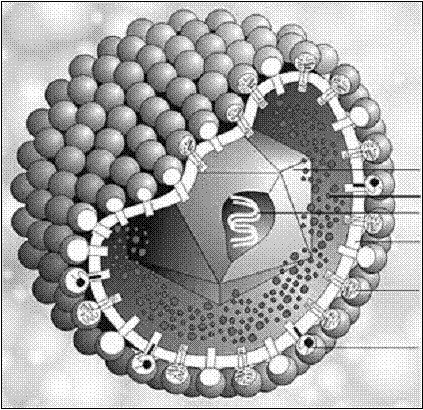
du document 1D :
Exemple
: virus de la grippe (famille orthomyxoviridae)
ARN
fragmenté et entouré de protéines : nucléocapside hélicoïdale
flexible (polymérase associée)
Protéine
M
tapisse la face interne de l’enveloppe (protéine de structure)
Peplos
(d’origine cellulaire) dans lequel sont ancrées 2 types de spicules :
*
Neuraminidase
: permet
d’atteindre les cellules cibles en hydrolysant l’acide sialique des mucoprotéines
protégeant l’épithélium respiratoire.
*
Hémagglutinines
: permettent la
reconnaissance et la pénétration intracellulaire, fixation du virus au globule
rouge => hémagglutination
223 – Les virus à symétrie mixte (ou complexes)
Analyse
du document 1E :
Exemple
du bactériophage
T4 infectant E.coli
Tête :
capside à symétrie cubique protégeant un ADN bicaténaire
Queue :
gaine contractile hélicoïdale
Spicules :
impliqués dans le phénomène d’adhésion à la bactérie
Crochets de
la queue
La
classification des virus reste beaucoup moins satisfaisante que celle des bactéries.
LHT
(LWOFF, HORNE, TOURNIER) vers 1960.
Cette
classification est remise à jour très régulièrement par le comité
international de taxonomie viral (CITV – internet )
La
classification des virus se fait selon 6 critères :
1) La nature de
l’acide nucléique : virus à ARN ou ADN
2) Le type de
symétrie de la nucléocapside (cubique, hélicoïdal)
3) L’absence ou la présence
d’une enveloppe (virus nus
ou virus enveloppés)
Ces
trois critères permettent de définir la famille
=> - viridae
4) Le
nombre de capsomères dans
le cas de virus à symétrie cubique ou diamètre de la nucléocapside dans le
cas d’un virus à symétrie hélicoïdale
5) Caractéristique du génome
(masse moléculaire de l’acide nucléique, fragmentation, linéarité,
circularité ...), provenance de
l’enveloppe (membrane cytoplasmique cellulaire ou membrane nucléaire
cellulaire. On définit là le groupe ou le genre.
6) Différents
sérotypes, pouvoir pathogène, épidémiologie etc.
On
définit alors l’espèce ou la sous espèce.
Non
officielle mais couramment utilisée par les cliniciens. Cette
classification est basée sur le type d’hôte, les effets pathologiques,
les modes de transmission....
Exemples :
-
virus entérique
-
virus respiratoire
-
virus oncogène => tumeurs chez hôte
On
classe en :
* Famille => commence par une
majuscule + suffixe “viridae ”
* Genre => commencent par une
majuscule et finit par “virus”
* espèce => minuscule
Remarque :
De nombreux virus sont nommés sous forme d’acronymes : VZV, HBV, VIH en
français etc.
4 – La multiplication virale :
Du
fait de leur parasitisme absolu les virus ne peuvent se multiplier
qu’au sein d’une cellule hôte. Il est donc nécessaire qu’il y ait interactions
virus – cellules.
Cependant,
pour qu’il y ait multiplication virale, il faut :
-
Un virus complet et fonctionnel
-
Une cellule compétente : c'est-à-dire capable d’assurer la
totalité des étapes du cycle viral
41 – Définition :
La
multiplication virale regroupe tous les évènements qui vont de
l’adsorption du virus sur la cellule cible jusqu'à la libération des
nouveaux virus.
42 – Les grandes étapes du cycle de multiplication :
421 – l’absorption :
Cette
étape, obligatoire pour qu’il y ait infection, consiste en une interaction
entre les protéines virales de surface et des récepteurs cellulaires spécifiques.
Cette reconnaissance de récepteurs cellulaires explique pourquoi certain virus
sont spécifiques d’espèces et de cellules.
422 – La pénétration et la décapsidation :
Suite
à l’adsorption, on assiste à la pénétration du virus dans la cellule soit
par une vacuole d’endocytose soit par fusion de l’enveloppe
virale avec la membrane cellulaire. La nucléocapside libère ensuite l’acide
nucléique : c’est la décapsidation. Il n’y a aucun signes
visibles de l’infection virale
423 – La phase de réplication :
On
assiste :
-
à la réplication du génome viral
-
à l’expression des gènes viraux et à la synthèse des protéines
virales
-
à l’assemblage des protéines de la capside
Ces
étapes sont très différentes en fonction des virus.
424 – La maturation et la sortie des virus :
Les
génomes viraux sont encapsidés et les nouveaux virus sont libérés
soit par lyse de la cellule hôte pour les virus nus soit par
bourgeonnement pour les virus enveloppés.
43
– Exemples de cycles de multiplication virale :
431
– Les virus à ADN :
DOC
3A Exemple : Virus de
l’herpes, ADN double brin linéaire, symétrie cubique, enveloppé, il infecte
les neurones sensitifs de la peau.
Après
adsorption, fusion enveloppe - membrane cytoplasmique, pénétration puis décapsidation,
l’ADN viral parvient dans le noyau et commande la synthèse de protéines
virales précoces. Une ADN polymérase virale réplique alors le génome un
grand nombre de fois. La transcription de ces nombreux génomes viraux donne
naissance aux ARNm tardifs puis après traduction aux protéines capsidiales.
L’encapsidation peut avoir lieu, l’enveloppe virale est formée au détriment
de l’enveloppe nucléaire et enfin les virus sortent de la cellule par de RER
et l’appareil de Golgi.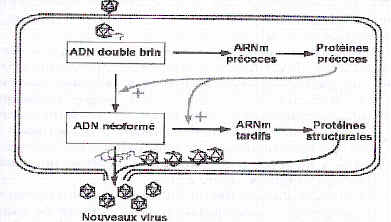
432
– Les virus à ARN (+) :
DOC
3B Exemple : poliovirus,
ARN + donc messager, nu, cible les motoneurones.
Adsorption
du virus et reconnaissance de récepteurs membranaires de surface. Pénétration
par une vésicule de pinocytose puis décapsidation dans le cytoplasme. L’ARN
+ viral va subir ensuite deux étapes :
-
Traduction cellulaire par les ribosomes et obtention d’une ARN polymérase
-
Réplication de l’ARN + en nombreux ARN -.
Ces
ARN – sont ensuite répliqués grâce à l’ARN polymérase en très nombreux
ARN+. Les nouveaux ARN+ sont traduits en protéines capsidiales puis encapsidés.
La cellule libère les nouveaux virus lorsqu’elle éclate.
433
– Les rétrovirus :
L’ARN
+ des rétrovirus n’est jamais utilisé comme ARN messager mais retrotranscrit
en ADN. Cet ADN s’intègre ensuite dans le génome de la cellule hôte sous la
forme d’un provirus. Les gènes viraux seront ensuite transcrits comme des gènes
cellulaires « normaux ».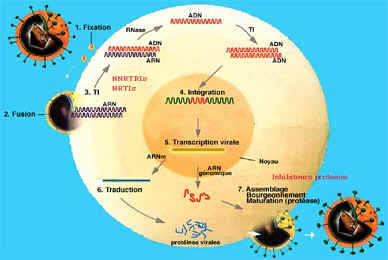
DOC
3D première partie
REMARQUE
importante :
La
cellule infectée a été TRANSFORMEE par l'ADN viral (Cf Griffith). Celle
cellule à 3 devenirs possibles :
-
Elle peut
produire de nouveaux virions qui iront infecter d'autres cellules
-
Elle se
multiplie, réplique son ADN ainsi que le provirus et le transmet donc à la
descendance
-
Elle peut
devenir cancéreuse : en s'intégrant dans l'ADN, le provirus dérègle les gènes
du contrôle cellulaire d’où prolifération anarchique de cellules infectées.
On parle de virus oncogènes (Ex HTLV1 et leucémies)
DOC
3D première partie
Exemple :
Virus VIH, ARN + mais non messager, enveloppé, ciblant les Lymphocytes T CD4+.
Après
adhésion des glycoprotéines virales aux récepteurs CD4 des lymphocytes T, le
virus pénètre par endocytose. L’ARN + est décapsidé, puis retrotranscrit
en ADN simple brin grâce à la reverse transcriptase apporté par le virus. Une
ADN polymérase cellulaire complète le brin d’ADN manquant et le double brin
s’intègre dans l’ADN cellulaire. Le provirus est alors transcrit comme un gène
cellulaire. Certains ARNm seront traduit en protéines virales (dont les GP 120)
et d’autres seront encapsidés. Les nouveaux virus sortent par bourgeonnement,
emportant une partie de la membrane cytoplasmique.
434
– Les bactériophages :
Exemple :
Bactériophage T4, d’E coli, ADN ds, symétrie mixte.
Les
bactériophages sont des virus qui infectent les bactéries DOC
3E 1ere partie.
Ces
bactériophages ont deux cycles de multiplication : DOC
3E 2eme partie
-
Cycle lytique : multiplication virale
-
Cycle lysogénique : intégration sous la forme de prophage
Applications :
vin, biologie moléculaire.
5
– Le pouvoir pathogène des principaux virus humains :
Cf
DOC : Il faut être capable d'associer Nom virus àmaladie
Conclusion :
D’où
proviennent les virus, comment sont ils apparus ?. Deux hypothèses :
-
Les virus les plus
sophistiqués proviendraient d’une évolution rétrograde au cours de laquelle
des cellules parasites se seraient simplifiées au point de devenir totalement dépendantes
de leur hôte. Théorie corroborée par les Mycoplasmes et les Rickettsies.
-
Il pourrait s’agir
d’acides nucléiques devenus indépendants en ayant acquis la faculté de
former des particules nucléoprotéiques et de s’envelopper.